
接上(第一篇)~
?
4、電化學表征
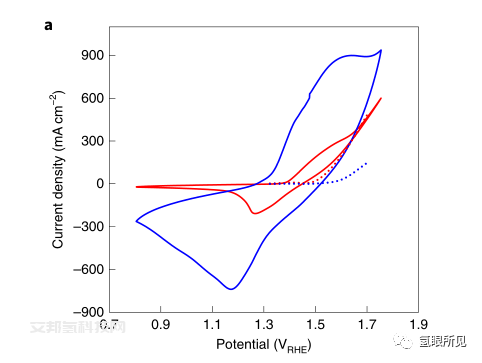
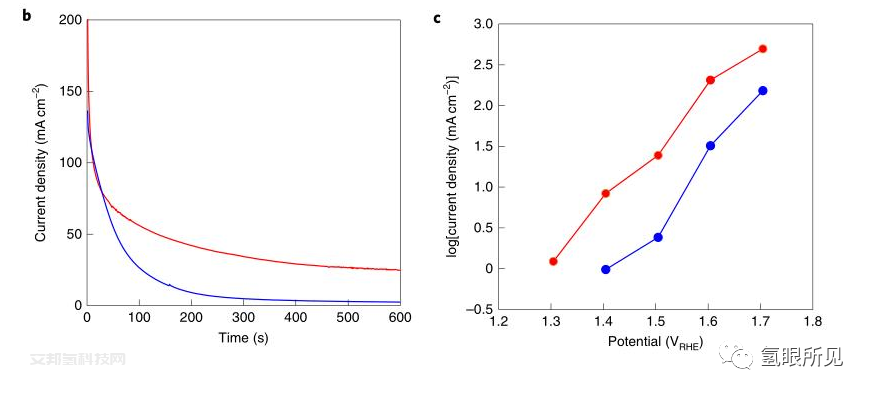
Ni0.9Co0.1(OH)2和NiFe LDH陽極的電化學性能說明:
圖a,在50 mV/ s的掃描速率下測量的循環伏安圖。
圖b,計時安培電流痕跡為1.48 VRHE。
圖c, Tafel圖是穩態水氧化電流與電位的函數,從10分鐘安培電流圖,如b中所示。
虛線a表示從c中提取的穩態水氧化電流。對于所有圖,Ni0.9Co0.1(OH)2陽極用藍色表示,NiFe LDH陽極用紅色表示。所有試驗均在5 mol/L KOH環境溫度下進行。
備注:塔菲爾(Tafel)圖是表示電極電位與極化電流或極化電流密度之間的關系。
?
為了確定Ni0.9Co0.1(OH)2陽極充電反應的法拉第效率,我們首先比較了電容電荷與計時安培充電過程中流動的總電荷。在1.48 VRHE的電位下對完全放電的陽極充電時,法拉第效率大于99.7%,持續時間超過2000秒,在此期間陽極充電超過50 C /cm2。為了驗證不產生氧氣,在1.48 VRHE恒電位下對完全放電的陽極充電時,監測電解液中的溶解氧濃度。在55 C/ cm2的電荷范圍內,沒有觀察到溶解氧濃度上升。
在盡可能類似于E-TAC工藝的產氫步驟的條件下(即在恒電流下給陽極充電),也對溶溶氧濃度進行監測。此外,在1.48 VRHE再生Ni0.9Co0.1(OH)2陽極時安培充電下,還測量了溶解氧濃度。在這兩種情況下,在3 C/ cm2以上的溶解氧濃度沒有上升,確認在這些條件下陽極充電時沒有產生氧氣。最后,氣相色譜測量顯示,在固定電流密度為50 mA/cm2(即充電5 C/ cm2)的情況下,陽極密封電池的頂空氫氣濃度上升,而氧氣濃度沒有上升。這些結果證實了在E-TAC制氫過程中,陽極充電時沒有發生析氧等寄生副反應。
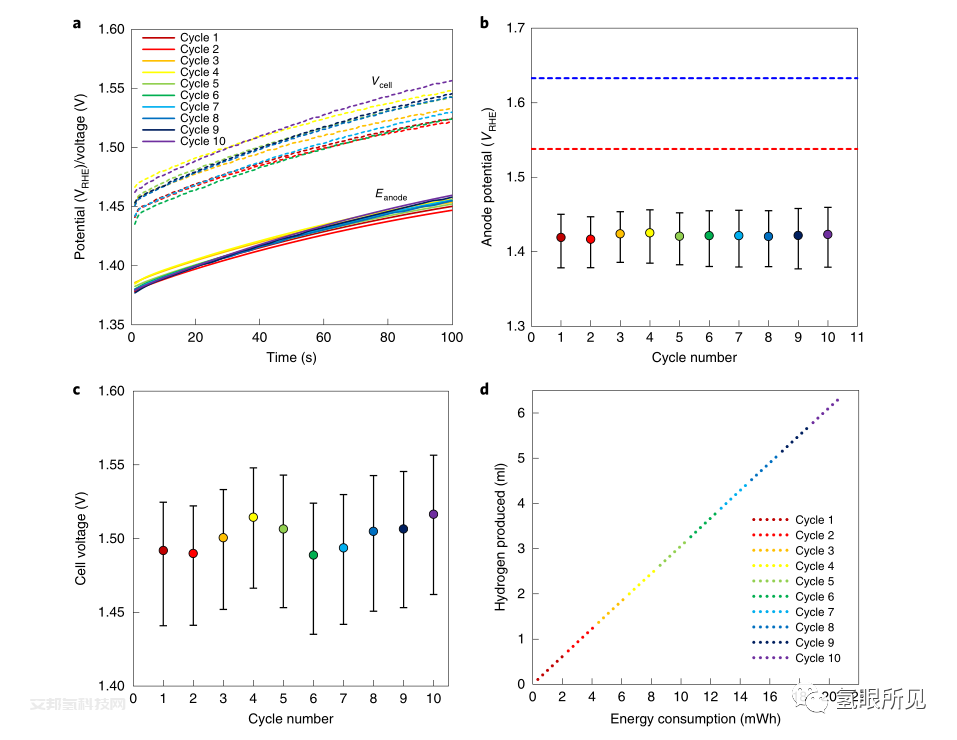
在E-TAC的概念驗證實驗中,氫氣在鍍鎳不銹鋼陰極上產生,而Ni0.9Co0.1(OH)2陽極在5 M KOH水溶液(pH 15)中氧化為Ni0.9Co0.1(OH)2。采用了Ni0.9Co0.1(OH)2陽極,再生容量為5 C/ cm2。產氫步驟在環境溫度下進行(不加熱或冷卻),電流密度為50 mA/ cm?2,時間為100 s。我們將施加的電池電壓限制在不超過120 mV的熱中性電壓(1.48 V)。這有助于最大限度地減少熱損失,并防止氧的產生和陽極過充,這可能使NiO(OH)從β相轉變為γ-p相。根據溶解氧測量,對于該電荷量,陽極充電反應的法拉第效率為99.2%±0.1%。在制氫(充電)步驟期間記錄了電池電壓Vcell和陽極電位Eanode,如下圖a所示:
每100 s產氫步驟結束后,將帶電陽極從冷電池中取出,置于熱(T = 95°C)電解液(5 M KOH)中100 s,以加速自發釋氧和初始狀態的再生。在陽極再生步驟中觀察到明顯的氣泡(O2)形成,而在氫氣生成步驟中,氣泡(H2)只在陰極上形成。
在每個充電步驟中,電池電壓和陽極電位以一致的方式增加,從一個循環到另一個循環顯示出很少的變化,沒有穩定的漂移(圖3a)。這種電化學行為表明,該過程是循環的,沒有降解;在每個循環結束時,陽極的SOC返回到初始狀態,沒有可測量的變化。為了證實這一點,在E-TAC循環之前、期間和之后,通過原位顯微結構(SEM)和結晶度(x射線粉末衍射)分析驗證了陽極的循環性。
在制氫步驟中,陽極電位從1.37-1.45 VRHE(下圖a)變化,遠低于Ni0.9Co0.1(OH)2和NiFe LDH陽極的OER電位(分別由下圖b中的藍色和紅色虛線表示)。在這些電位下,氧的析出可以忽略不計。電池總電壓從1.44-1.56 V變化(下圖a),在所有10個周期中平均為1.5 V(下圖c)。E-TAC過程的電壓效率36,Vth/Vcell,其中Vth為水裂解反應的熱中性電壓(標準條件下為1.48 V),在所有10個循環中平均為98.7%。由電流×時間乘積(即電荷)可以計算出,在下圖所示的十次循環中產生了6.4 ml氫氣(1 atm, 25°C),根據循環中測量的電流和電池電壓消耗20.8 mWh,如下圖所示。因此,E-TAC工藝實現了較低的電能消耗,僅為3.24 kWh /m3,或39.9 kWh/ kg氫氣。

7.碳酸鹽緩沖電解質溶液中的E-TAC水分解
因此,還通過在pH值為10.6的碳酸鹽-碳酸氫鹽(K2CO3:KHCO3的3:2比例)緩沖電解質中操作來證明該方法的多功能性。在該試驗中,在25 mA /cm2的標稱電流密度下,陽極電位從1.43–1.50VRHE變化。這表明E-TAC水裂解工藝不僅限于堿性溶液,在電化學工業中具有更廣泛的應用潛力。
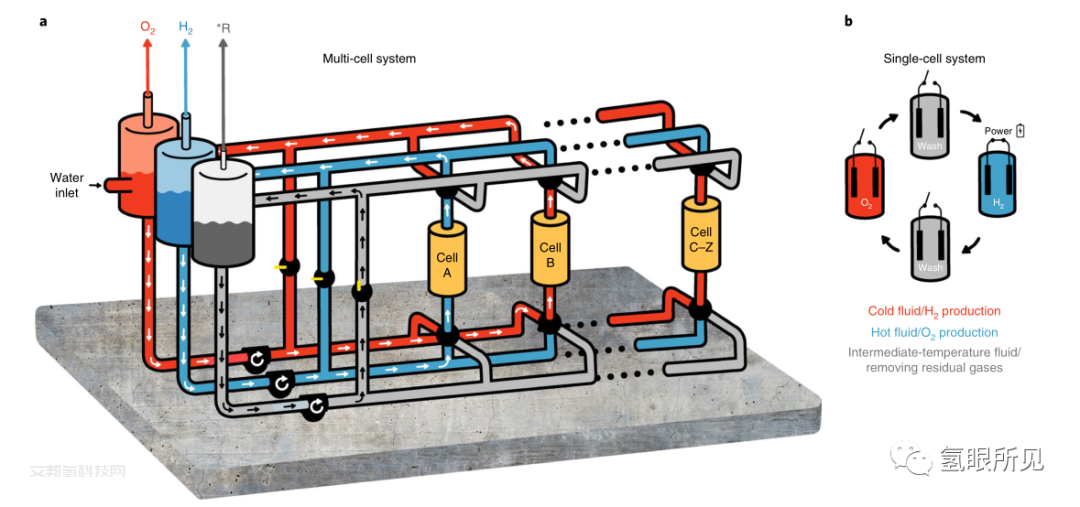
多單元E-TAC過程示意圖:
a,過程中一般的電解液流動,圖中為冷電解質在a槽內循環,產生左側中間(藍色)槽相分離的H2氣體,而熱電解質在B槽內循環,產生左側紅色槽相分離的O2氣體。左邊灰色槽中的中溫洗滌液大部分時間通過旁路循環。該液體用于將冷電解質溶液和熱電解質溶液“推”到生成H2或生成O2步驟結束時各自的槽中。
b,單電池循環,顯示每個電池的再生操作,H2在環境溫度下的電偏置下產生,O2在不施加電偏置的更高溫度下產生(開路)。
* R,表示殘余氣體。
?
未完待續,敬請期待~
原文始發于微信公眾號(氫眼所見):關于H2Pro這家電解水企業以及E-TAC技術路線的介紹(第二篇)
 艾邦氫能產業鏈通訊錄,目前有2200人加入,如億華通、清極能源、氫藍時代、雄韜、氫牛、氫璞、愛德曼、氫晨、喜馬拉雅、明天氫能、康明斯、新源動力、巴拉德、現代汽車、神力科技、中船712等等,可以按照標簽篩選,請點擊下方關鍵詞試試
資料下載:
艾邦氫能產業鏈通訊錄,目前有2200人加入,如億華通、清極能源、氫藍時代、雄韜、氫牛、氫璞、愛德曼、氫晨、喜馬拉雅、明天氫能、康明斯、新源動力、巴拉德、現代汽車、神力科技、中船712等等,可以按照標簽篩選,請點擊下方關鍵詞試試
資料下載:


