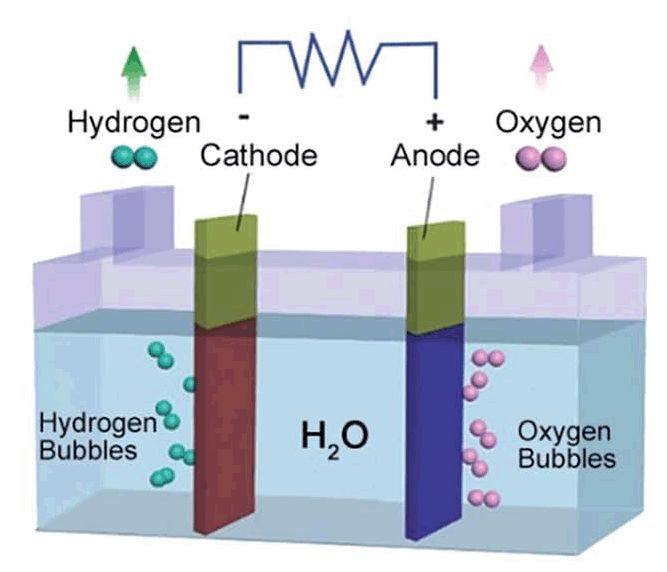
電解水時,質子或水合氫離子在陰極得到電子,發生還原反應,生成氫氣析出,該過程簡稱為氫還原反應(Hydrogen Evolution Reaction,HER)。HER反應在不同介質中反應過程也有所不同,從分子層面理解其詳細的機理有助于我們加深對電解水的整體認識,對于一線的科研工作者來說,還需熟悉表征該反應的相關參數指標。
本文深度科普HER反應的機理,并對各主要表征參數展開介紹,幫助大家從本質上加深對電解水析氫的理解。

-反應機理-
在酸性介質中,氫氣的生成需要兩步,首先是Volmer過程(式1),即水合氫離子結合電子生成活性氫原子H*吸附在活性物質表面(M)。第二步則有兩種方式,取決于H*生成與消耗的平衡關系:當H*的生成速率大于消耗速率時,活性物質表面H*過量,此時兩個H*易于直接結合,生成氫氣,稱為Tafel過程(式2);另一種是Heyrovsky過程(式3),即當H*的生成速率小于消耗速率時,一個H*與質子和電子結合,生成氫氣。
H3O+ + e- + M → MH*+ H2O (Volmer) (1)
2MH* → 2M + H2(Tafel) (2)
MH* + H3O+ + e- → M + H2+H2O (Heyrovsky) (3)
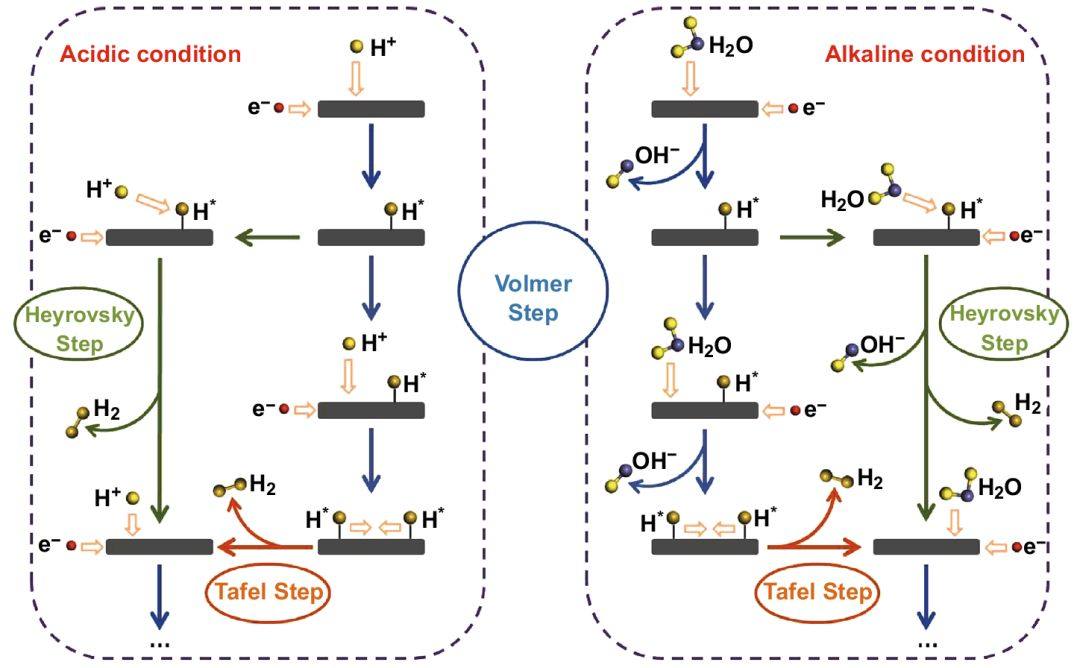
酸性(左)和堿性(右)介質中的HER機理
在堿性介質中,質子濃度大幅降低,因此Volmer過程和Heyrovsky過程發生變化,Volmer過程中,水和電子結合,生成吸附氫原子和氫氧根離子(式4);Heyrovsky過程則是吸附氫原子結合一個水分子和一個電子,生成氫氣和氫氧根離子(式5)。
M + H2O + e- → MH* + OH-(Volmer) (4)
MH* + H2O + e- → M + H2 + OH-(Heyrovsky) (5)

-表征參數-
E = Eθ - RT/nF·ln CRb/COa (6)
R——氣體常數,8.314 J·mol-1·K-1;
F——法拉第常數,8.314 J·mol-1·K-1;
具體到氫還原反應,公式(6)變為以下形式(式7):
E = Eθ -RT/nF·ln(1/c(H+)2) (7)
理論上,外加電勢超過反應的平衡電極電勢反應即可發生,但實際上由于反應活化能的存在,需要額外的外加電勢才能使反應發生并持續進行,即過電勢η(式8):
η = E測 - E (8)
氫還原反應的標準電極電勢規定為0,即Eθ = 0。值得注意的是,測試所得極化曲線通常會進行電勢的校正,即去除溶液電阻所導致的電勢差。此外,還需根據所選參比電極的標準電極電勢(vs. RHE),將電勢轉化為對氫電極電勢,經轉換后的對氫電極電勢的計算方程式如下(式9):
ηRHE = E測 - E + E參 - IR (9)
ηRHE = E測 + E參 - Eθ + RT/nF·ln(1/c(H+)2)- IR (10)
為實現低成本高效率的電解水制氫,需要在低過電勢下達到高電流密度。通過測試采集催化材料的極化曲線,可得到電流密度隨電勢變化的信息,目前普遍以電流密度達到-10mA/cm2 (η-10)所需的過電勢作為指標,衡量材料的催化HER性能。
| 塔菲爾斜率 |
在實際應用中,電流密度與過電勢的關系可用Butler-Volmer來表達(式11):
j = j0 {exp[(1-α)nFη/RT]- exp(-αnFη/RT)} (11)
式中: j0——交換電流密度 (mA/cm2);
α——對氧化反應和還原法反應偏向程度的不對稱系數。
對于氫還原反應,在高過電勢下,方程簡化為Tafel公式(式12):
j ? - j0 exp(-αnFη/RT) (12)
構造描述電流密度與過電勢的函數,將此函數定義為Tafel斜率b為(式13):
b = 2.303RT/αF (13)
根據該函數可知,b越小,電流密度隨過電勢增大而增大的越快,因此可作為反映材料的催化性能的指標。
此外,在HER中,Tafel過程和Heyrovsky過程往往共同發生。可根據塔菲爾斜率判斷反應的動力學過程,推斷決速步驟:當Volmer過程為決速步驟時,b接近118 mV/decade;Tafel過程為決速步驟時,b接近39 mV/decade;Heyrovsky過程為決速步驟時,b接近29 mV/decade。
| 氫吸附吉布斯自由能 |
由反應機理可知,無論在酸性還是堿性介質中,H*作為產氫的中間產物參與了所有過程的反應,因此活性物對H*的吸附能 (△GH*) 對材料的催化HER性能有著重大影響。當以交換電流密度來反映材料的催化性能,以交換電流密度和△GH*為坐標軸作圖,即可得到“火山圖”。該圖表明,鉑(Pt)的△GH*接近于0,具有最大的交換電流密度,表明Pt具有最好的催化HER性能。位于Pt右側的材料對H*的吸附過弱,難以穩定生成H*,而位于左側的材料對H*吸附過強,產生的H2難以脫附,會封閉活性位點,因此,隨著△GH*向左右兩側逐漸遠離0,交換電流密度也隨之減小。該結果證明△GH*接近于0的催化材料由于對H*的吸附力適中,最適合作為HER高效催化劑。
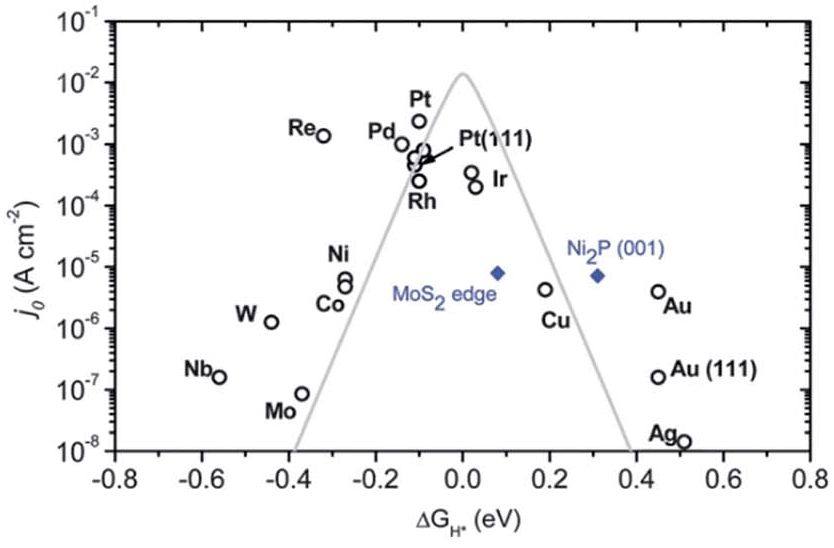
交換電流密度與△GH*的火山圖
| 穩定性 |
持續穩定催化的能力是檢驗催化劑的重要指標。檢驗方法主要有兩種,一是在恒電壓下測試電流隨時間的變化曲線(I-t曲線),通常持續測試12 h以上,曲線顯示電流無明顯衰退,則認為催化劑的穩定性良好;另一種是測試初始極化曲線和持續工作一定時間后的極化曲線,對比前后曲線的差異,如測試后曲線顯示性能無明顯衰退,則認為催化劑的穩定性良好。
圖靈科創官網:http://www.sztlkc.com/
原文始發于微信公眾號(圖靈科創):電解水氫還原反應機理及有關參數








