?? ? 隨著氫能的不斷探索開發,相關制氫的技術也有很多,但在很多實驗過程中發現產氫量超過了大家計算的理論值,這些實驗大家有人認為是失敗,或者由其他因素會有影響。如今我們開始從事PEM電解水的開發研究過程中同樣也發現了采用排水法測量的氫氣也超過了大家計算的理論值,于是我們通過多次實驗排出了各個問題,還是發現產氫量的結果差異不大,測試結果為11ml/min*A*cm2。我重新整理計算了理論產氫量,則發現與大家計算的結果有差異,以下為我們的計算過程,如有問題請指正。
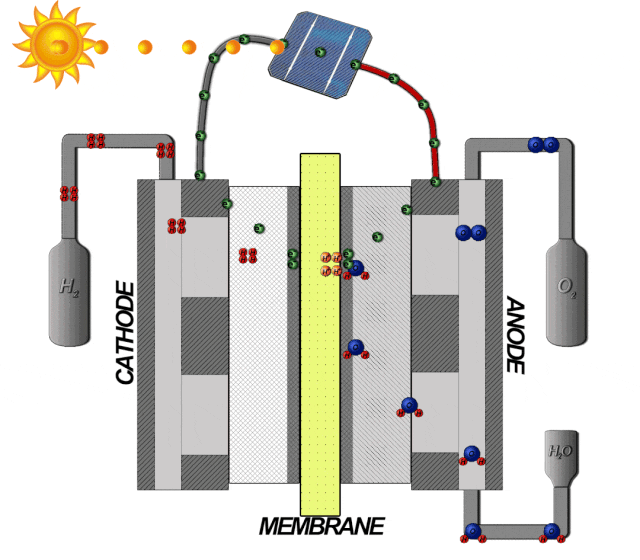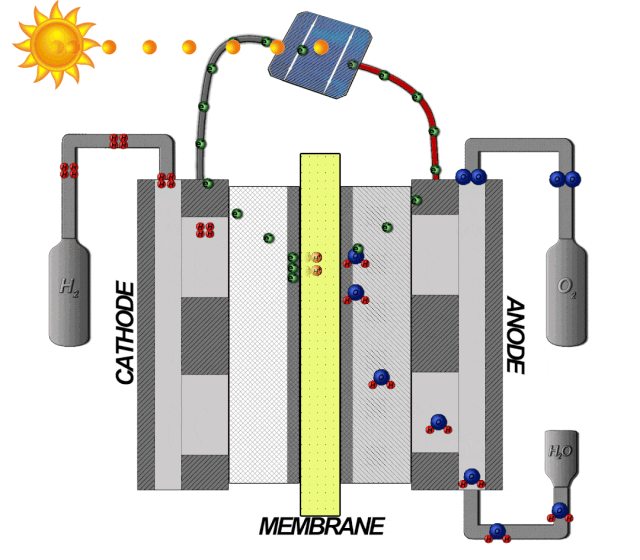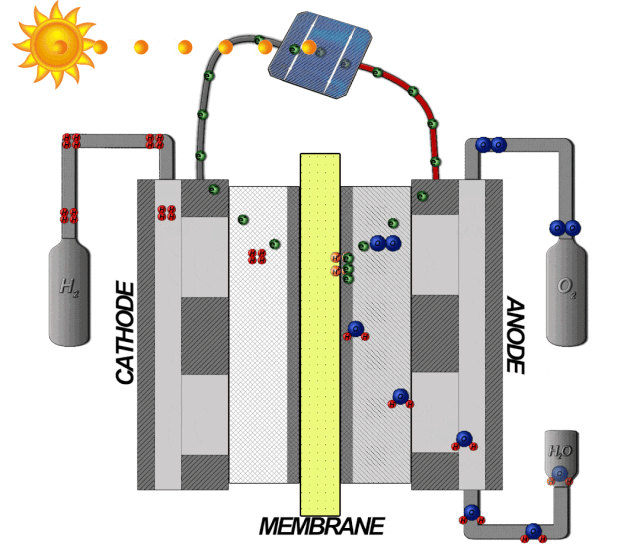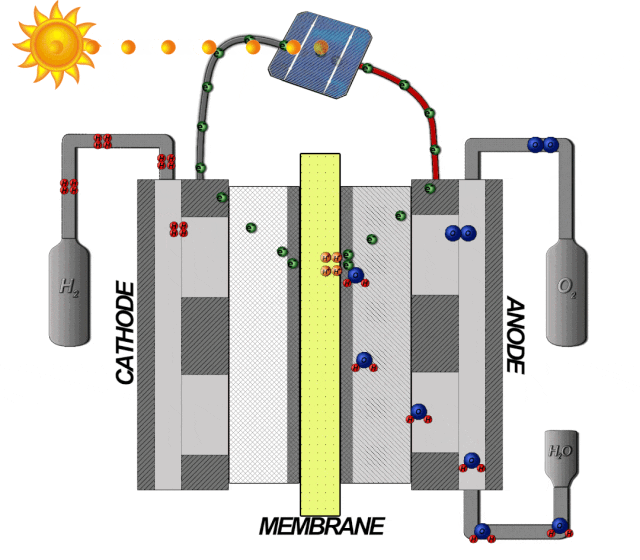
根據電解水制氫的反應式為:
2H2O+2e=2H2+O2;H2O+e=H2+O2/2
? ?通過上式可知1個水分子+1個電子分解為1個氫分子+1/2個氧分子,通常我們是給PEM電解槽通的是直流電,按照上海澎藍測試數據為1.65V/cm2*A為例,該參數表示每平方厘米通過1A電流是電解槽電壓為1.65V。那么這里我們便以1A的電流計算每平方厘米的產氫量。
? ?那么安培與電子之間的轉換關系為 :
1A=1C/s (C為庫倫數)
? ?庫倫的定義:若導線中載有1安培的穩定電流,則在1秒內通過導線橫截面的電量為1庫侖。
? ?一個電子所帶負電荷量e=1.602176634×10-19庫侖,也就是說1庫侖相當于6.24150974×1018個電子所帶的電荷總量。
? ?通過以上定義我們可以看出通過1cm2面積的電子速度為于6.24150974×1018(個/s);
? ?根據電解水制氫的反應式H2O+e=H2+O2/2,也就是說理論上有6.24150974×1018(個/s)電子參與反應生產了氫氣,那么氫氣的數量應該為6.24150974×1018(個/s)氫分子產生(根據反應式這些電子其實供給了氧分子形成了共價鍵,氫氣用的電子來源于水里的電子)。
? ?氫分子數量計算出來了,那我們如何轉換為我熟悉的ml/s或者ml/min,這里我們引進摩爾的定義——國際計量大會通過決議,1摩爾將定義為“精確包含6.02214076×1023個原子或分子等基本單元的系統的物質的量”。與此同時確定了阿伏伽德羅常數NA為6.02214076×1023。
1cm2產生的氫氣摩爾=氫分子數量/摩爾數
? 1cm2產生的氫氣摩爾=
6.24150974×1018(個/s)/ 6.02214076×1023個/mol
=1.0362×10-5mol/s
? ?查資料可知:氫氣的摩爾質量為2g/mol,那么
1cm2產生的氫氣摩爾x摩爾質量=1cm2產生的氫氣質量流量
1.0362×10-5mol/s×2g/mol
=2.0724×10-5g/s=0.020724mg/s
=1.24344mg/min
氫氣的密度為0.089kg/m3=0.089g/L=0.089mg/ml,那么1cm2產生的氫氣體積流量為:
1cm2產生的氫氣體積流量=1cm2產生的氫氣質量流量/氫氣密度
1.24344(mg/min)/0.089(mg/ml)=13.971ml/min
? ? ?以上為理論產氫量,那么我測試的結果為11ml/min*A*cm2,則轉換效率為:
11/13.971=0.7874=78.74%
?

?
原文始發于微信公眾號(澎籃氫能):PEM電解水制氫產氫量計算


