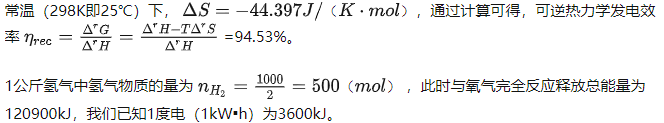?
?
?
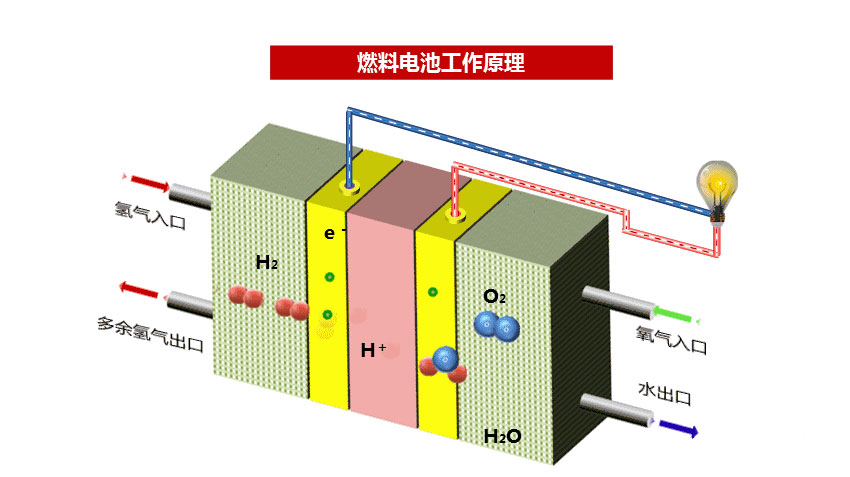
電化學反應發電本質上是基于氧化還原反應的電荷轉移,氣態水變液態水的過程沒有什么貢獻,因此,氫氣發電要用低熱值。
?
根據熱力學第二定律:不可能制成一種循環動作的熱機,從單一熱源取熱,使之完全變為功而不引起其它變化(開爾文表述),即不可能把1公斤氫氣和氧氣燃燒放出來的熱量全都用來作功(變成電能)而不引起變化。
?
這個變化,正是以“熵”為特征的熱。因此,任何裝置使用化學能(燃料)發電作工,都有一個天然的極限轉換效率。
?
對于燃料電池來說,即可逆熱力學發電效率,就是燃料電池能達到的最高理論發電效率。
?
常溫(25℃)下,理論上1kg氫氣可以發500mol*241.8/3600kJ=33.58度電;按照目前燃料電池系統額定工況發電的最高額定效率算(60%,已包含可逆熱力學效率),實際上1kg氫氣可以發500mol*241.8/3600*60%=20.15度電。
?
電化學反應過程中是存在損耗的,主要來源于反應過程中的極化現象,包含歐姆極化,電化學活化極化和氣體擴散極化(濃差極化)。電化學效率是衡量燃料電池電堆技術水平的關鍵。
?
燃料參與反應的比例。有的燃料電池可以通過循環泵,把流過電堆但沒有參與反應的燃料再次循環利用,所以利用率就會很高,但也會有損失;有的燃料電池把沒有參與反應的燃料給燒掉,以熱能形式輸出,此時燃料利用率就只能算參與反應的比例。
?
?
水管理、熱管理、氣體(氫氣、空氣)供應、控制-電管理等子系統部件需要消耗一定的能量(電或熱)。
?
?
比如常見的高溫燃料電池——固體氧化物燃料電池(SOFC)和熔融碳酸鹽燃料電池(MCFC)——工作溫度高達600~1000℃,排出的氣體都會有高品位余熱,可用于家庭、商業場所、公共單位的熱水供應、冷鏈、生鮮超市、數據中心的高溫蒸汽聯合制冷機制冷。
熱電聯供往往是高溫燃料電池才有的技能,常見的低溫燃料電池,如質子交換膜燃料電池(PEMFC)和堿性燃料電池(AFC),相對來說,回收熱能十分有限。
?
 艾邦氫能產業鏈通訊錄,目前有2200人加入,如億華通、清極能源、氫藍時代、雄韜、氫牛、氫璞、愛德曼、氫晨、喜馬拉雅、明天氫能、康明斯、新源動力、巴拉德、現代汽車、神力科技、中船712等等,可以按照標簽篩選,請點擊下方關鍵詞試試
資料下載:
艾邦氫能產業鏈通訊錄,目前有2200人加入,如億華通、清極能源、氫藍時代、雄韜、氫牛、氫璞、愛德曼、氫晨、喜馬拉雅、明天氫能、康明斯、新源動力、巴拉德、現代汽車、神力科技、中船712等等,可以按照標簽篩選,請點擊下方關鍵詞試試
資料下載: