
一、電解單元基本原理
圖1中的概念單元可以很容易地轉化為具有實際意義的電解水單元。在這種電池中,操作時氣體(H2和O2)在兩個界面上都會產生。要避免的第一個問題是氣體(溶解在電解質中或以氣泡的形式)的相互運輸和它們的自發重新組合,這可能導致爆炸危險,同時也會造成重大的效率損失。解決這個問題的辦法是在電解質中兩個電極之間放置一個電解單元隔膜。隔膜需要有足夠的多孔性,以便讓離子自由地貫穿整個隔板,但不能太多,以避免氣體從隔膜的一側轉移到另一側。另一個重要的約束來自于氣泡由于密度和重力等問題并會沿每個界面向上流動的事實,這就導致了滲透。當工作電流密度增加時,這可以導致形成連續的、高阻的氣體薄膜,從而增加電解單元阻抗。解決這個問題的一個辦法是使用多孔電極(例如,網格或毛氈結構),并將它們壓在電解單元隔膜上,以迫使氣體排出到后方,在那里它們可以通過強制電解質循環以被自由收集。另一種更復雜的設計是將隔膜和電解單元電解質的作用結合到一個單一結構中(可以是浸漬液體的聚合物)電解質或離子導電聚合物或離子導電陶瓷),以擺脫循環電解質。當離子導電聚合物被用作電解質時,這種類型的電池有時被稱為“固體聚合物電解質”(SPE)電解槽。
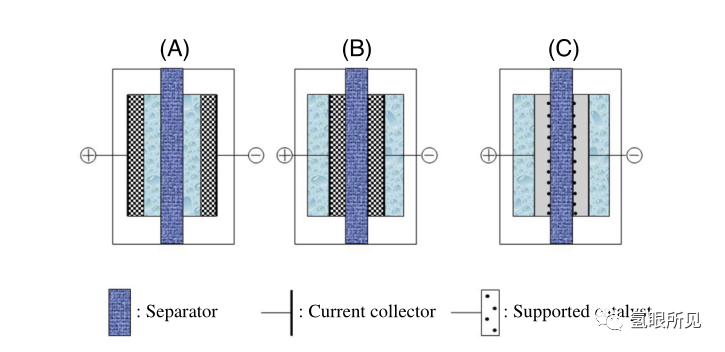
圖1:電解單元的主要構造
二、電解液pH值的作用
水電解槽可用于電解液態水或水蒸氣。在1bar壓力下,液態水電解池的工作范圍為0°C(融冰溫度)- 100°C(水蒸氣生成溫度)。實際上,由于動力學原因,沒有必要冷卻一個水電解池,并在低于標準值(25°C)的溫度下工作。通常電解液態水發生在50℃以上(以降低電池阻抗),在90℃以下(電解單元材料穩定性的限制)。利用自加壓電電解單元,液態水的存在范圍可擴展到100℃以上。但是有一個限度,超過這個限度只有水蒸氣才能被電解。這種操作條件稱為近環境溫度和壓力(NATP)操作條件。電解液態水可以使用PH值介于0(強酸)和14(強堿)之間的任何電解質來進行。實際上,由于電荷載體的存在,沒有必要使用中性電解質。為了提高電解單元的效率,最好使用更多的可移動離子,即質子(因此有必要使用強酸性的水溶液電解質)或羥基離子(因此有必要使用強堿性的水溶液電解質)。即使羥基離子的遷移率比質子的遷移率低約16倍(由于特定的跳躍傳輸遷移機制或Grotthuss機制,質子具有較高的遷移率),這可以通過使用高濃度KOH水溶液在一定程度上加以平衡。
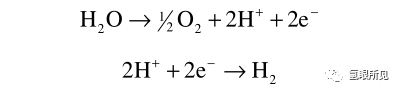
在堿性水溶液條件下,電解水反應的半反應為:
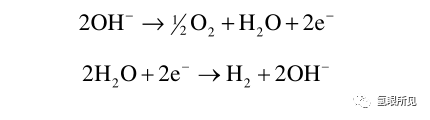
這些半單元反應的pH依賴性如下圖2所示。
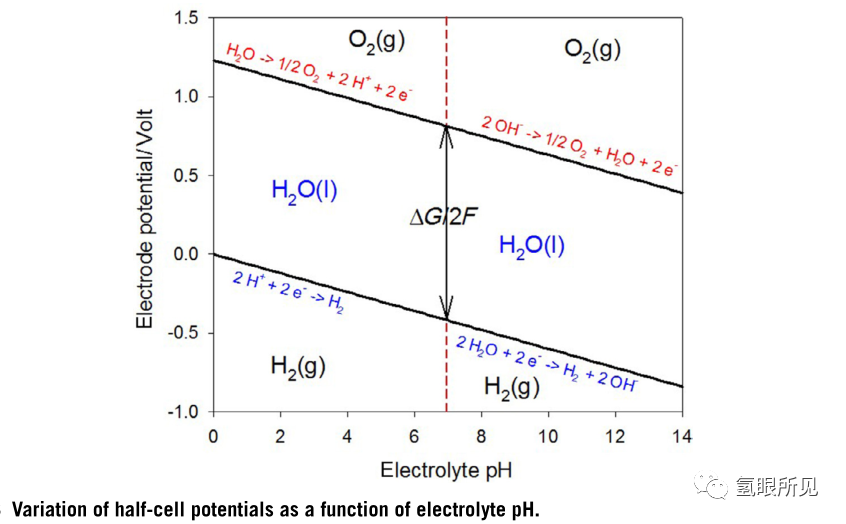
圖2:半單元電位隨PH值的變化
在堿性介質中,電極電位沿電位軸向下移動到ph電位鈍化區域,在該區域過渡金屬受到保護。因此,廉價的過渡金屬可以用作催化劑和電解單元組件。當電解液酸化時,電極電位向上移動到PH電位跨鈍化區域,在該區域過渡金屬不再受到保護。在酸性介質中,耐酸材料如鉑族金屬作為電催化劑是必需的。此外,將圖1(C)所示的SPE與電解質一起使用,而不是使用循環酸電解液,以避免腐蝕問題,以及組件、管道和BOP組件所使用昂貴的材料。決定使用配備酸性或堿性電解質的電解槽取決于幾個因素,這些因素近來已經被討論和驗證。
1、根據圖1(C)的設計,給出了限制電解質的電解單元的原理。這種限制通常是通過使用離子導電聚合物(離聚體)來實現的。質子導電(圖3A)和羥基離子導電(圖3B)聚合物都可以用于這一目的。使用質子導電聚合物作為“固體電解質SPE”的水電解電池通常被稱為PEM電池(PEM代表質子交換膜)。在這種材料中,可以達到非常大的質子活性,相當于1 M硫酸水溶液,但這些質子仍然被困在宿主基質中,因為陰離子反離子以共價鍵結合在聚合物主鏈上,不能促進離子電荷的傳輸。羥基離子導電聚合物也可用于水電解應用。使用羥基導電聚合物作為“固體電解質SPE”的水電解池通常被稱為AEM (AEM代表陰離子交換膜)。如果膜的電導率太低,可以通過在細胞內循環或多或少濃度的KOH溶液來提高膜的電導率。

圖3:A/B:PEM和AEM電解單元示意圖
2、下圖4為常規堿水電解槽的原理圖。這是一個間隙電池(圖1A所示),其中氣體在電極和中央隔膜之間演化,因此導致電流密度的限制。

圖4:堿性電解單元示意圖
3、使用聚合物電解質的電池的操作范圍可以擴大到幾百攝氏度,但通常是通過浸漬非揮發性酸,如磷酸來實現的。在300°C到600°C之間,存在空隙,幾乎沒有離子導電材料。在600°C以上,可以使用氧離子導電陶瓷作為電解單元隔膜和電解質。在這種材料中,離子載流子是氧離子(O2?)。電解水反應的半反應為:
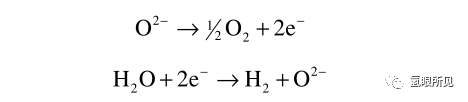
下圖5是SOWE(固體氧化物水電解)的原理圖。陽極或陰極支持的薄電解質層的發展對效率的提高作出了顯著的貢獻。
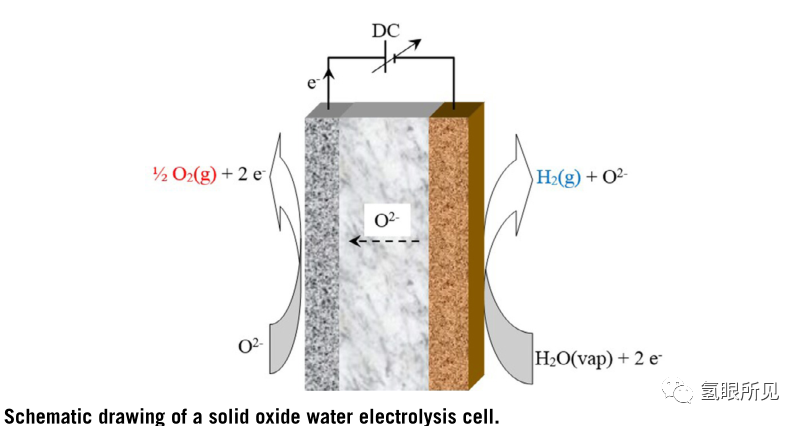
圖5:固體氧化物電解單元
原文始發于微信公眾號(氫眼所見):水電解槽的一些基本理論淺述


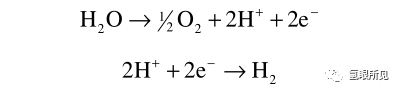
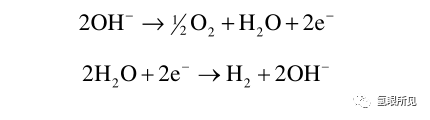



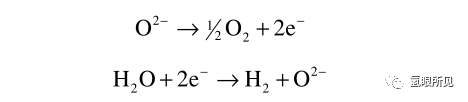

 艾邦氫能產業鏈通訊錄,目前有2200人加入,如億華通、清極能源、氫藍時代、雄韜、氫牛、氫璞、愛德曼、氫晨、喜馬拉雅、明天氫能、康明斯、新源動力、巴拉德、現代汽車、神力科技、中船712等等,可以按照標簽篩選,請點擊下方關鍵詞試試
資料下載:
艾邦氫能產業鏈通訊錄,目前有2200人加入,如億華通、清極能源、氫藍時代、雄韜、氫牛、氫璞、愛德曼、氫晨、喜馬拉雅、明天氫能、康明斯、新源動力、巴拉德、現代汽車、神力科技、中船712等等,可以按照標簽篩選,請點擊下方關鍵詞試試
資料下載:
 艾邦氫能產業鏈通訊錄,目前有2200人加入,如億華通、清極能源、氫藍時代、雄韜、氫牛、氫璞、愛德曼、氫晨、喜馬拉雅、明天氫能、康明斯、新源動力、巴拉德、現代汽車、神力科技、中船712等等,可以按照標簽篩選,請點擊下方關鍵詞試試
資料下載:
艾邦氫能產業鏈通訊錄,目前有2200人加入,如億華通、清極能源、氫藍時代、雄韜、氫牛、氫璞、愛德曼、氫晨、喜馬拉雅、明天氫能、康明斯、新源動力、巴拉德、現代汽車、神力科技、中船712等等,可以按照標簽篩選,請點擊下方關鍵詞試試
資料下載:



