氫眼所見尋找有緣的氫能人,有緣之人可添加微信“zen13480834343”
最近,又看到一些關于H2Pro這家企業以及E-TAC(電化學-熱活化化學)水分解法制氫的一些信息,今天就針對這家企業以及該技術路線做一些簡單分析。
一、關于H2Pro這家企業
-
在2019年1月份,由馬爾科(Talmon Marco)以色列理工學院的三位氫能領域專家(分別為:Hen Dotan博士、Gideon Grader教授和Avner Rothschild教授)共同創辦。(這位馬克也快被媒體神化成馬斯克一樣了......)

-
該公司主要是基于E-TAC技術進行制氫設備開發。該技術是以色列理工大學通過電化學—熱活化水分解技術可以解耦此過程,并以98.7%的能量效率顯著提升氫氣的生產效率。該文章已發表在2019年9月的Nature Energy。
-
目前該公司已經獲得韓國現代、比爾蓋茨名下Breakthrough Energy Ventures,李嘉誠名下維港投資等等知名機構的投資。
-
企業目標,基于E-TAC技術的高電解效率來實現低成本的綠氫。
二、E-TAC技術的說明
1.關于E-TAC基本介紹
通過將電解水過程分為兩個步驟來解耦這些反應:一個是電化學步驟,在陰極還原水并氧化陽極;然后是一個自發的化學步驟,在更高的溫度下加快速度,通過氧化水將陽極還原到初始狀態。這使得在無膜雙電極電池中,在平均電池電壓為1.44–1.60 V、標稱電流密度為10–200 mA/cm2的情況下,整體水分裂成為可能。這使我們能夠在低電壓下以簡單、循環的過程生產氫氣,具有高效率、穩健性、安全性和規模化放大潛力。(貌似電流密度不高)
E-TAC是一種解耦水分解的方法,克服了實現電解水制氫的能量轉換效率的重大障礙。在此過程中,在實現的方案中提供了更多的自由度,使工藝參數的優化超過了傳統的電解槽。
E-TAC通過將水的氧化反應分為兩個步驟來實現:一個是電化學步驟,氧化陽極;然后是一個自發的化學步驟,通過氧化水將陽極還原到初始狀態:
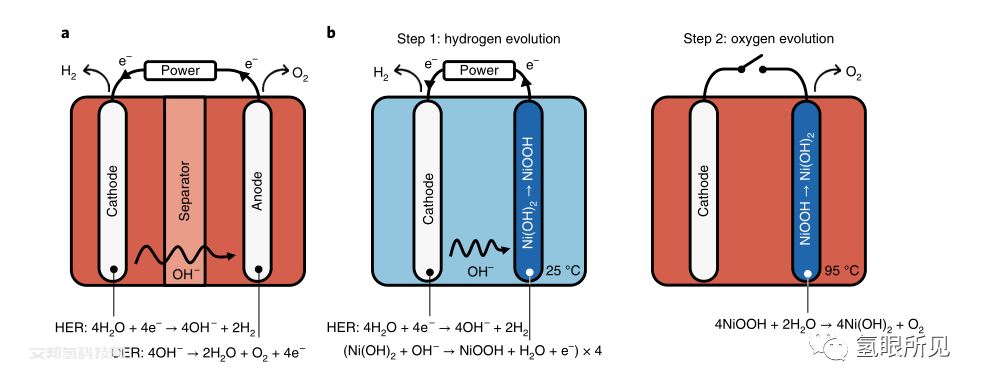
我們開發的工藝如圖1所示,它比較了傳統堿水電解(下圖a)和我E-TAC提出的工藝(下圖b)。氫氣形成反應(在水分解的情況下析出氫)在這個方案中是不變的,因為它發生在陰極,而E-TAC只修改了在陽極的水氧化反應。因此,在第一個過程中,水在陰極被還原為氫氣,釋放出OH-離子。四電子析氧反應(OER)發生在常規電解的陽極(如下圖a),但在E-TAC中被分為兩個連續的步驟,包括四個單電子的氫氧化鎳(Ni(OH)2)陽極氧化反應步驟1,然后就是自發的析氧和陽極再生在熱活化的化學步驟,如下圖b所示(參見補充注釋1和補充圖1了解更多細節)。
因此,在E-TAC的兩步電化學-熱激活化學(E-TAC)循環中,當氧化陽極(現在是氧化氫氧化鎳(NiO(OH)))在自發的、釋放能的化學反應中還原為Ni(OH)2時,O?O鍵在第二步中形成,產生氧氣并再生陽極,完成整體的水分解反應。類似于自然系統中的氧演化復合物,該方案使用四個金屬中心來存儲氧化等價物,這有助于平衡基本氧化反應的電位,從而降低整體反應的過電位。與之前在此新興領域的其他研究工作相比,E-TAC的方法實現了解耦水分解,提高了效率和通用性,如下圖所示。

堿水電解及E-tAC水裂解工藝示意圖說明:
a,在堿性水電解中,通常發生在高溫下(50-80°C), OER和HER在時間和空間上是耦合的,因為它們同時發生在陽極和陰極,它們一起放置在同一個電池中。隔膜或陰離子交換膜將陽極和陰極分隔開,防止O2/H2交叉。
b、E-TAC拆分水分為兩個連續步驟進行:
Step1:電化學步驟(左)通過常規的HER在陰極還原水,釋放氫氧根離子(OH -),將氫氧化鎳(Ni(OH)2)陽極氧化成氧化氫氧化鎳(NiO(OH))。
Step2:熱化學步驟(右),即NiO(OH)陽極與水反應自發產生氧氣。
備注:第一反應(電化學)發生在環境溫度(~25°C),而第二反應(化學)在升高的溫度(~95°C)進行,以獲得最佳的反應速率;第一反應和第二反應之和為整體的水分解反應,2H2O→2H2 + O2。

3.電極設計
簡而言之,E-TAC水分解工藝用兩步循環取代了傳統的堿法電解水氧化反應,即陽極首先帶電(電化學),然后再生(熱化學)。第一步的析氫反應(HER)與傳統堿性電解過程相同,不同的是它發生在環境溫度(25°C)而不是高溫(通常為50-80°C)。因此,在傳統堿法電解中使用的陰極材料,如Raney鎳(雷尼鎳))或其他HER催化劑,都可以在E-TAC的工藝中使用。在前期的E-TAC項目驗證中使用鍍鎳不銹鋼網狀陰極作為標準基準的HER陰極進行的概念驗證實驗。
在E-TAC的工藝中,陽極的功能與傳統的堿性電解完全不同,需要仔細材料選擇和優化。陽極的關鍵選擇標準包括:在堿性溶液中的穩定性;金屬氫氧化物和氫氧化物系的循環性;氧化還原電位高于可逆OER電位(1.23 VRHE)低于氧在陽極材料上的演化電位;高容量;充電速度快,再生速度快。這些考慮都指向了Ni(OH)2/ NiO(OH)陽極,由于其可循環性和高能量密度,它們通常用于堿性二次電池。Ni(OH)2按以下反應可逆地氧化為NiOOH : Ni(OH)2 + OH -?NiO(OH)+ H2O + e-。
雖然Ni(OH)2/NiO(OH)標準氧化還原電位比可逆OER電位高190 mV,但其過大的過電位在動力學上抑制了OER。這使得堿性電池在不過度充電的情況下,可以運行數千次,而不會產生寄生氧進化,從而導致膨脹和故障。為了抑制過度充電時可能發生的寄生氧析出,使用了催化Ni(OH)2/NiO(OH)反應并抑制氧析出的添加劑,最常用的添加劑之一是鈷。鈷提高了陽極的電子和質子電導率,并使Ni(OH)2/NiO(OH)氧化還原電位發生陰極偏移,擴大了充電和過充電之間的電位窗口。因此,與未摻雜鈷的Ni(OH)2相比,Ni1-xCox(OH)2陽極可以以較低的電位帶電,從而達到較高的荷電狀態(SOC),而不需要氧的析出。
與應避免產生氧氣的電池陽極不同,該工藝的陽極必須在E-TAC循環的第二步中產生氧氣。此外,在產氫(第一步)過程中,抑制伴隨氧析出的自發再生反應是必要的。因此,E-TAC設計的陽極和操作條件是為了在第一步抑制氧的析出,在第二步促進氧的生成。該實驗驗證使用以Ni0.9Co0.1(OH)2為陽極,采用電化學浸漬(ECI)法制備在泡沫鎳基底上。ECI電極比燒結或粘貼電極具有更高的表面積,因此可以在較低的過電位下保持較高的電流密度。此外,與粘貼的電極相比,ECI電極的再生率要高得多。在泡沫鎳基體上覆蓋了一層約9 μm厚的β-氫氧化鎳層。通過能量色散光譜測定涂層成分,得到Ni:Co的比例為6.7:1.0(其中x?0.1;即Ni0.9Co0.1(OH)2)。
原文始發于微信公眾號(氫眼所見):關于H2Pro這家電解水企業以及E-TAC技術路線的介紹(第一篇)





 艾邦氫能產業鏈通訊錄,目前有2200人加入,如億華通、清極能源、氫藍時代、雄韜、氫牛、氫璞、愛德曼、氫晨、喜馬拉雅、明天氫能、康明斯、新源動力、巴拉德、現代汽車、神力科技、中船712等等,可以按照標簽篩選,請點擊下方關鍵詞試試
資料下載:
艾邦氫能產業鏈通訊錄,目前有2200人加入,如億華通、清極能源、氫藍時代、雄韜、氫牛、氫璞、愛德曼、氫晨、喜馬拉雅、明天氫能、康明斯、新源動力、巴拉德、現代汽車、神力科技、中船712等等,可以按照標簽篩選,請點擊下方關鍵詞試試
資料下載:


